生細胞は、細胞膜上の受容体タンパク質(リセプター)を介して外部からの化学的・物理的シグナルを細胞内へと伝達し、周囲の環境変化に柔軟に対応しています。したがって、これらの動的なシグナル伝達の生物学的役割を解明するには、任意のタイミング・場所でシグナル伝達を調節する技術が必要です。ここではリセプターを介した化学的・物理的シグナル伝達を光により制御するツールを紹介します。
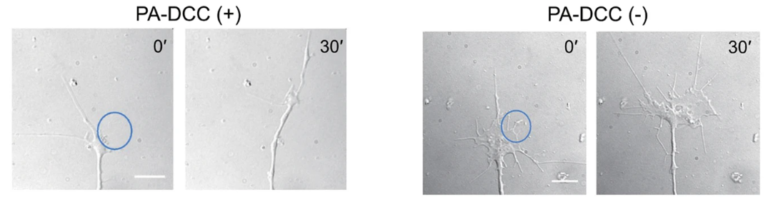
化学的シグナル伝達を担うリセプターのなかには、リガンド分子の結合による二量体・多量体形成が活性化につながるものが多く存在します。例えば軸索誘導を担うリセプターであるDCCは、リガンド分子netrin-1の結合によるDCCの多量体形成が活性化を引き起こすことがわかっています。そこで本研究室では、青色光照射により多量体を形成するCRY2をDCCのC末端側に融合することで光応答型分子PA-DCCを作成しました。PA-DCCは光照射によるCRY2の多量体形成により融合しているDCCが多量体を形成し、活性化します。本分子を神経細胞に導入することで、線虫体内での神経軸索の伸長方向を光で誘導することに成功しました。
細胞間で働く物理的シグナル伝達として、細胞間の張力伝達が代表的です。細胞膜タンパク質E-cadherinは細胞間接触面で隣接細胞上に発現するE-cadherinと複合体を形成し、細胞内で相互作用しているactomyosin複合体で発生した収縮力を隣接細胞に張力として伝達することが知られています。そこで本研究室では、光照射により切断されるタンパク質PhoClをE-cadherinの細胞内ドメインに融合した光切断型分子PC-Cadherinを作成しました。PC-Cadherinは光照射によるPhoClの切断によりE-cadherin細胞内ドメインが切断されます。結果として、E-cadherin複合体を介した張力伝達を光依存的に阻害することが可能となります。
また、細胞膜上のリセプター量は生体内で厳密に制御されていることが知られています。例えば代表的なリセプターであり薬剤標的としても重要なGPCRは、リガンド分子の結合後、細胞質側でβ-arrestinと相互作用し、エンドサイトーシス経路で細胞内に取り込まれることがわかっています。そこで本研究室では、青色光照射依存的に相互作用するタンパク質CRY2/CIB1のペアを活用し、GPCRのひとつであるβ2アドレナリン受容体(ADRB2)とβ-arrestin 2との相互作用を光依存的に引き起こすツールを開発しました。本ツールにより、ADRB2の取り込みにはβ-arrestin 2との相互作用が十分であることや、相互作用の長さにより取り込み後の経路が変化することが明らかとなりました。
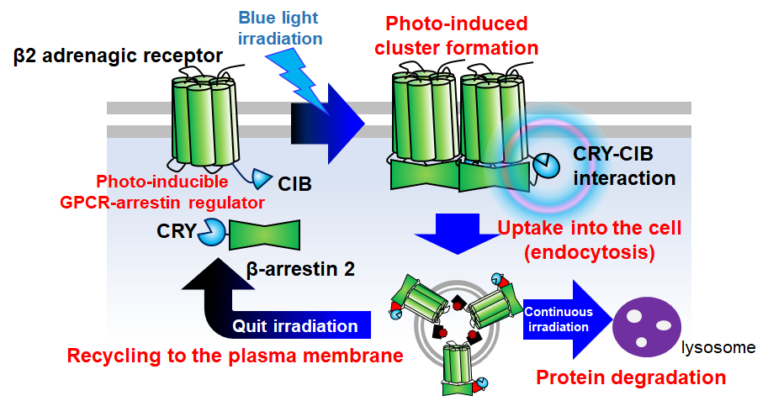
このような細胞膜リセプターの光操作原理は様々なリセプターに活用することができ、生体内におけるリセプターを介した動的な細胞間シグナル伝達の生物学的役割の解明に貢献すると期待されます。
- M. Endo, T. Iwawaki, H. Yoshimura, T. Ozawa, ACS Chemical Biology. 14, 2206–2214 (2019).
- O. Takenouchi, H. Yoshimura, T. Ozawa, Scientific Reports. 8, 677 (2018).
- M. Endo, M. Hattori, H. Toriyabe, H. Ohno, H. Kamiguchi, Y. Iino, T. Ozawa, Scientific Reports. 6, 23976 (2016).
